OPRD综述:P-手性二氢苯并氧磷杂环戊烷磷配体促进的催化与合成(上篇)[1]


OPRD综述:P-手性二氢苯并氧磷杂环戊烷磷配体促进的催化与合成(上篇)[1]

膦配体是过渡金属催化的化学反应中非常重要的一类配体,能与Pd、Rh、Ru、Ir等多种过渡金属搭配使用,催化各种各样的化学转化。手性膦配体则广泛应用于各种不对称反应中。根据手性来源不同,手性膦配体可分为两种类型:具有手性骨架的手性膦配体和具有P-手性的手性膦配体。由于手性磷原子能与过渡金属配位,将手性环境传递到靠近金属中心的位置,而这通常是反应中心,因此P-手性配体在催化过程中往往具有非常优异的表现。这使得自从P-手性配体被发现以来就受到化学家的广泛关注和深入研究,目前已有一大批优秀的P-手性配体被发展出来,并在工业生产(尤其是制药行业)中发挥了重要的作用。
在众多P-手性配体中,近十几年来发展出了一类独特的、其基本母核含有P-手性二氢苯并氧磷杂环戊烷结构的P-手性配体,如图1所示。这类膦配体的反应活性和选择性已在众多化学转化中得到充分的验证。其具有以下特点:1)这类配体结构刚性,且大多数较为富电子,因此在交叉偶联和氢化反应中能促进氧化加成和还原消除环节,从而有利于推进反应进行;2)由于P-手性二氢苯并氧磷杂环戊烷的刚性很强,因此在不对称催化过程中构象明确;3)P-手性二氢苯并氧磷杂环戊烷的可修饰位点众多,能灵活的调整配体的电性和空间位阻,进而改变配体手性口袋的形状、深度及电性,最终针对不同的底物和反应达到理想的催化效果;4)此类配体大多对空气稳定,便于在工业生产中操作、使用;5)此类配体能实现公斤级以上生产,满足工业生产的需要。
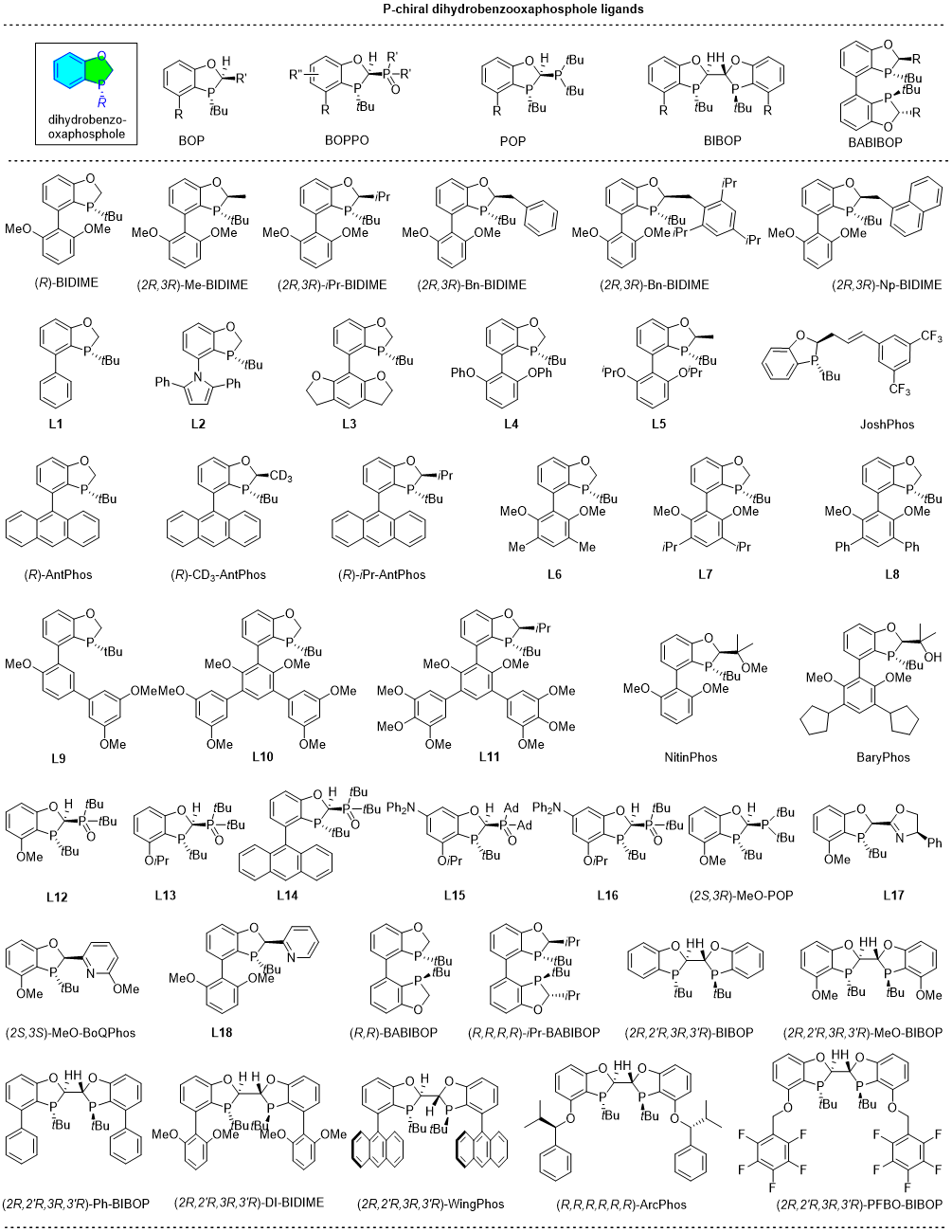
图1.P-手性二氢苯并氧磷杂环戊烷类膦配体
近日,绍兴赜军生物医药科技有限公司在Organic Process Research & Development(OPRD)期刊发表综述文章,系统总结了P-手性二氢苯并氧磷杂环戊烷类型的磷配体在各种反应中的应用,包括在天然产物和药物分子合成中的应用(doi:10.1021/acs.oprd.4c00064)。本文参考此综述,结合原文献,筛选其中在工业上较为常用的反应做一个简单的探讨,本文主要介绍P-手性二氢苯并氧磷杂环戊烷类磷配体在非手性 Suzuki偶联、手性 Suzuki偶联中的应用情况。
1
非手性 Suzuki偶联类
1.1 芳基-芳基Suzuki-Miyaura偶联
如图2所示,以rac-BIDIME或rac-AntPhos为配体,在Pd催化下能实现大位阻的芳基-芳基Suzuki偶联,获得一系列邻位三取代或四取代的联芳基类化合物。该方法具有产率高,官能团普适性强,催化效率高等优点:对于邻位具有异丙基、叔丁基等位阻极大的官能团能实现高效偶联;适用于萘环、蒽环等并环骨架底物;对于吡唑、恶唑、吡啶、异喹啉等杂环底物也有很好的催化效果;药物分子中常见的氰基、硝基、醛基、三氟甲基、磷酰基等官能团也能很好的兼容(图2A)。2017年,BI公司的研究团队发现,在非离子表面活性剂Triton X-100的存在下,使用BIDIME为配体,能在水中进行ppm级的Pd催化芳基-芳基Suzuki偶联,并在50g级规模上以几乎定量的收率合成了一个11-β-HSD-1抑制剂(图2B)。rac-BIDIME在连续流反应中也有应用,能满足大位阻、多杂环底物的Suzuki偶联,并在克级规模上得到验证(图2C)。基于上述优点,BIDIME和AntPhos在含有多取代联芳基药物中具有很大的应用潜力。
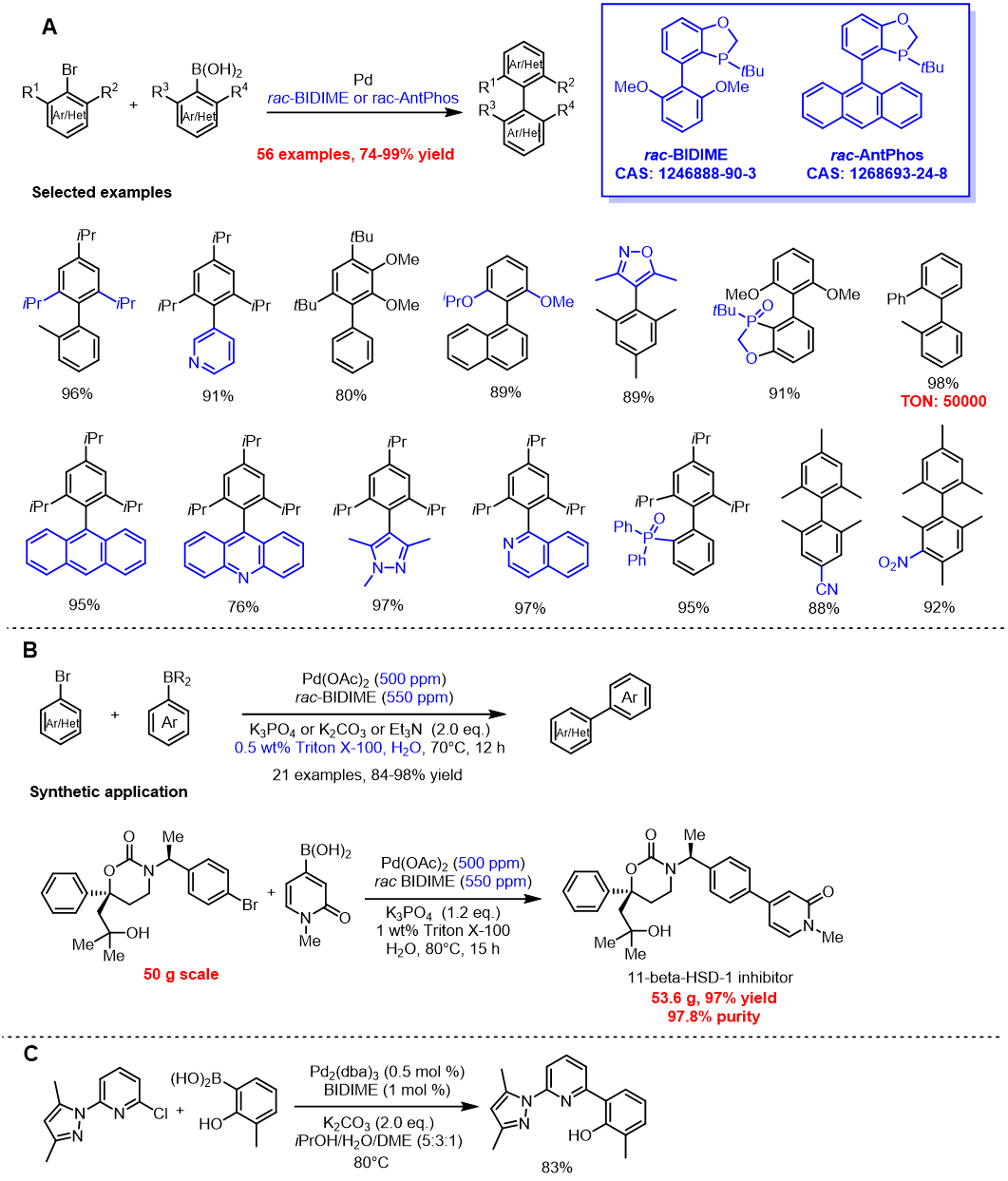
图2. 以BIDIME或AntPhose为配体的大位阻Suzuki-Miyaura偶联[2-5]
1.2 芳基-烷基Suzuki-Miyaura偶联
不同于上述的芳基-芳基Suzuki偶联,芳基-烷基Suzuki偶联是一类难度更大却同样很重要的偶联反应。尤其是邻位双取代芳基卤化物与烷基硼酸(或硼酸酯)的偶联更是需要克服巨大的困难才能实现:首先两个偶联片段都存在较大的位阻,不利于偶联的发生;其次,烷基硼酸存在β-氢,容易发生β-氢消除。AntPhos和BOPPO类型配体L12成功克服了上述难点,为大位阻芳基-烷基偶联提供了方法。AntPhos能实现邻位二取代芳基卤代物与一系列环状二级硼酸化合物的偶联,相应的三元环、四元环、五元环、六元环硼酸类底物均可采用该方法实现偶联,该方法强大的偶联能力在合成两种齿轮状分子中得到充分的体现(图3A);L12则完成了邻位二取代芳基卤代物与非环状二级硼酸底物的高效偶联,能通过偶联在芳环上引入异丙基、异丁基及含苯基等官能团的长碳链等大位阻官能团,萘环、蒽环等并环骨架也能兼容,游离胺基、硝基、氰基、烷氧基等活泼基团亦不受影响(图3B)。

图3.大位阻邻位二取代芳基卤代物与烷基二级
硼酸底物的高效Suzuki-Miyaura偶联[6-8]
2
手性 Suzuki偶联类
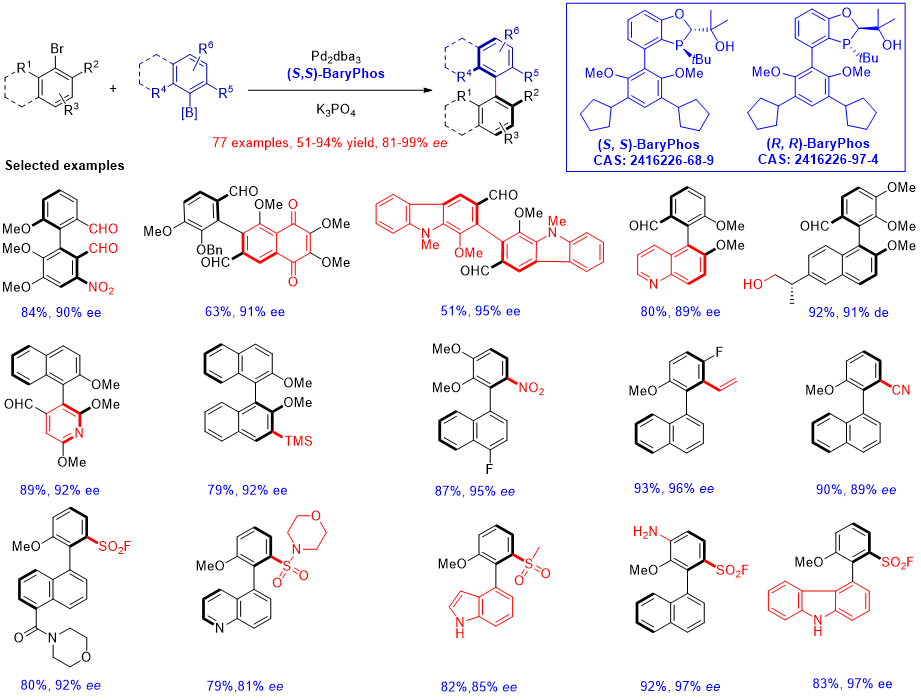
图4. BaryPhos 介导的不对称芳基-芳基交叉偶联
在BIDIME的氧磷杂环片段中氧、磷原子之间的亚甲基上引入不同的取代基,可以获得一系列由BIDIME衍生的P-手性配体。这些配体能实现多种高度官能团化的轴手性联芳基化合物的构建,并在复杂天然产物全合成中得到充分的应用,论证了其实用性,如图5所示。以Me-BIDIME为催化剂,可实现芳基硼酸与邻位含有苯并恶唑烷酮取代的芳基溴的高效不对称偶联;而Np-BIDIME则可介导芳基硼酸与邻位含磷酸酯的芳基溴进行不对称偶联,产物ee值最高可达96%[9]。进一步研究研究发现在Pd-iPr-BIDIME体系的催化下,该方法能很好的适用于邻位含羟基的联芳基轴手性化合物的合成,羟基上的保护基具有导向作用,对反应的对映选择性影响巨大,多种官能团化的轴手性连、联芳基化合物均可在此催化体系下合成。以此方法合成轴手性中间体作为关键步骤,研究团队顺利完成了复杂天然产物korupensamine A 和B,将这两个天然产物进行偶联,最终完成了具有强抗HIV活性的天然产物Michellamine B的简洁合成[10],展示了该方法在药物合成中的实用性。

图5. Pd/BIDIME促进的不对称Suzuki-Miyaura
偶联及其在复杂天然产物中的应用[9,10]
BI公司的研究团队在合成一个含有轴手性、结构复杂的HIV整合酶抑制剂时,报道了以(S)-BIDIME为配体构建关键轴手性的例子。由于两个偶联片段均较为复杂,且偶联步骤处于合成路线的后期,偶联效果的好坏将极大的影响药物的成本,研究团队筛选大量配体后,最终确认(S)-BIDIME为最佳配体,在温和条件下能实现两个片段的高效偶联,产物经重结晶后可以达到73%的收率、90%的de值,体现了BIDIME在轴手性药物合成中的高效性和实用性(图6A所示)[11]。Johnson & Johnson公司的MCL-1抑制剂JNJ-4355是一个大环联芳基类候选药物,此分子最大的结构特征之一为轴手性是其唯一的手性,而该轴手性对其分子特性影响巨大,如何高效构建此轴手性是合成该候选药物最关键的步骤,在筛选大量的配体后最终ent-L7显示了最好的催化效果,以96%的产率,76 : 24的er值获得目标产物,尽管对映选择性未达到最理想效果,但已经极大的提高了后续的拆分效率和产率,减少珍贵产品的浪费(图6B所示)[12]。
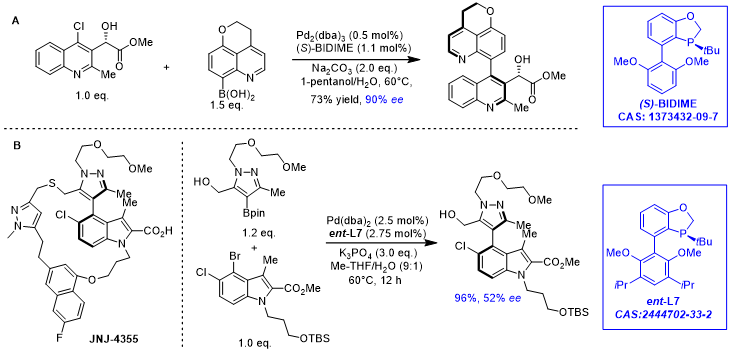
图6. Pd/BIDIME类型配体催化的不对称芳基-芳基偶联在药物合成中的应用
BIDIME及其衍生产品构成了一类结构特异、功能强大的P-手性单膦配体,在Suzuki-Miyaura偶联方便展示了独特的优势,具有选择性好、催化剂载量低、底物普适性广、反应条件温和、大部分产品对空气稳定、操作便捷等优点,在手性和非手性Suzuki-Miyaura偶联中都得到了广泛的应用,在药物分子的合成中正发挥越来越重要的角色。目前绍兴赜军医药科技有限公司已实现多种BIDIME类型膦配体年数十公斤级的供应能力,产品面向全球。
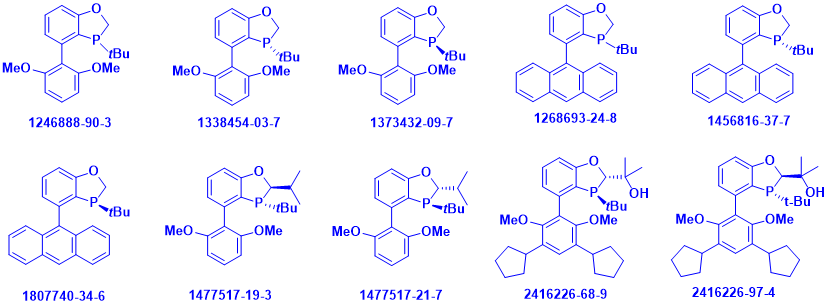
图7. 赜军医药科技有限公司的特色单膦配体(部分)
下期推文,我们将介绍P-手性二氢苯并氧磷杂环戊烷磷配体在不对称氢化中的应用。
参考文献:
1. 10.1021/acs.oprd.4c00064
2. Angew. Chem., Int. Ed. 2010, 49, 5879-5883.
3. Chem. Eur. J. 2013, 19, 2261-2265.
4. Asian J. Org. Chem. 2017, 6, 1285-1291.
5. J. Org. Chem. 2019, 84, 4926-4931.
6.Org. Chem. Front. 2014, 1, 225-229
7. Angew. Chem., Int. Ed. 2015, 54, 3792-3796.
8. Org. Biomol. Chem. 2017, 15, 9903-9909.
9. Org. Lett. 2012, 14, 2258-2261
10. J. Am. Chem. Soc. 2014, 136, 570-573.
11. Angew. Chem., Int. Ed. 2015, 54, 7144-7148.
12. ACS Catal. 2022, 12, 8380-8385.
*更多产品信息,请访问:www.zejunpharma.com










